Nowoczesne podejścia w leczeniu próchnicy: biomimetyka i materiały bioaktywne
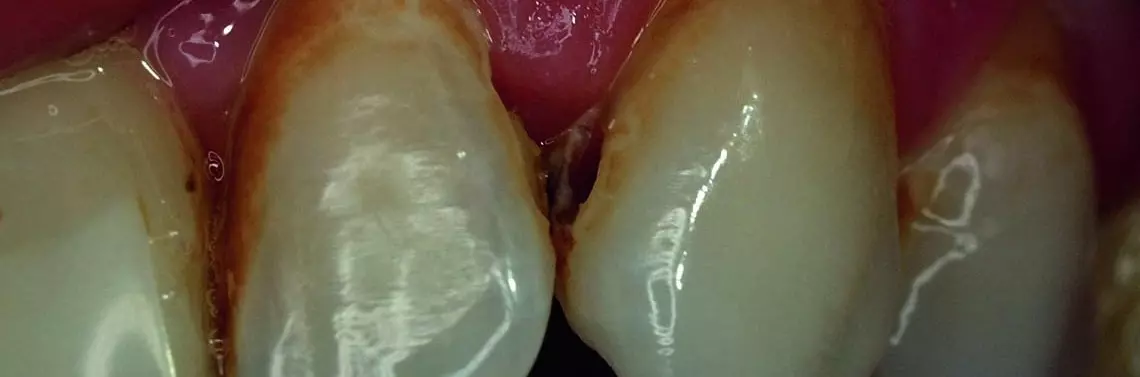
W zakresie leczenia próchnicy ubytkowej i nieubytkowej znajdziemy coraz szerszą gamę możliwych do zastosowania rozwiązań – od tradycyjnych dla materiałów bioaktywnych wykorzystujących przewagę stężenia jonowego i indukowania odpowiedzi tkankowej, poprzez niejako odwrócenie tej zasady, jak ma to miejsce przy stosowaniu monomeru peptydu P10-4, który czynnie pochłania jony z otoczenia, remineralizując ogniska w fazie przedubytkowej. Postępowanie opisywane jako terapia biomimetyczna przy prawidłowym realizowaniu zaleceń powinno powodować odtworzenie kryształów hydroksyapatytu w obrębie ogniska demineralizacji, a zewnętrzne stosowanie materiałów bioaktywnych istotnie zwiększa skuteczność postępowania. W świetle dostępnych publikacji z uwzględnieniem czasu obserwacji i liczby opracowań wskazuje się ostrożnie, że metoda staje się alternatywna dla dotychczasowych, opartych na remineralizacji i stosowaniu związków fluoru.
POLECAMY
Wypełnienia
Po naruszeniu ciągłości powierzchni konieczne staje się opracowanie ubytku i odtworzenie braku utraconych tkanek twardych. Uzyskanie wypełnienia – rekonstrukcji o właściwościach biomimetycznych, estetycznych, pożądanej odporności na czynniki panujące w jamie ustnej z uwzględnieniem aktu żucia – stanowi ogromne wyzwanie. Materiały stomatologiczne ewoluują wielokierunkowo, z uwzględnieniem składu i rodzaju monomerów, napełniaczy i dalszych licznych składników. Uzyskane w toku tej ewolucji materiały pozwalały na odtworzenie utraconych tkanek z pełnym przywróceniem funkcji, w tym estetyki. Rekonstrukcja taka (wypełnienie) była jednak pasywna względem tkanek, zapewniała przy prawidłowym postępowaniu szczelną obturację.
Historia rozwoju wypełnień
Poszukiwanie tworzyw aktywnie wspierających leczenie próchnicy ubytkowej jest nierozerwalnie związane z rozwojem stomatologii minimalnie inwazyjnej. Ograniczenie zakresu preparacji, ograniczenie traumatyzacji i jatrogenii wymaga odpowiedniego wsparcia materiałowego. Poszukiwanie tworzyw, które oprócz tego, że będą się charakteryzowały biozgodnością, zapewnią aktywne działanie na tkanki naturalne, obejmowało wiele różnych materiałów i modyfikacji już istniejących rozwiązań. Ciekawostką ostatnich lat może być próba zastosowania napełniaczy o właściwościach piezoelektrycznych. Oby pomysłodawcom coś zaiskrzyło.
W początkach lat 70. pierwsze kroki w kierunku bioaktywności wypełnień zapewniły szkło-jonomery, choć pamiętać należy, że również stare cementy krzemowe uwalniały fluor. Przełom w jakości i działaniu cementów szkło-jonomerowych nastąpił dopiero po zastosowaniu do ich budowy zmodyfikowanych szkieł. Istotny postęp zrozumienia działania szkieł bioaktywnych w wypełnieniach zawdzięczamy materiałom zwierającym szkła strontowe. Obecność tego pierwiastka umożliwiała ocenę zakresu dyfuzji w strukturze tkanek twardych.
Problemem „wczesnych” cementów G-J była wrażliwość na niskie pH, niska wytrzymałość mechaniczna oraz niezadowalająca estetyka. Dostępne obecnie materiały to efekt licznych udoskonaleń i modyfikacji. Dodatkowym wspomagającym rozwiązaniem jest stosowanie precyzyjnie skomponowanych lakierów, choć dla produktów takich jak G-Coat Plus (GC) bardziej poprawne będzie określenie „modyfikator warstwy wierzchniej”. Naniesienie preparatu na powierzchnię cementu szkło-jonomerowego powoduje penetrację i de facto wytworzenie powłoki kompozytowej wzbogaconej o nanowypełniacz wchodzący w skład G-Coat. Nadal pozostajemy jednak w strefie cementów szkło-jonomerowych.
Kompozyty
Przechodząc do materiałów, które mieszczą się w grupie kompozytów, należy omówić jeden z najpopularniejszych (jak wynika z zestawienia dystrybutora) materiałów, jakim jest Activa Bioactive Restorative. Tu jednak natychmiast trzeba wspomnieć, iż producent – firma Pulpdent – niechętnie odnosi się do takiego zaszeregowania, sugerując odrębną dla tego tworzywa nazwę: „bioaktywny materiał wypełnieniowy”. Odnosząc się do szczegółów budowy, składu, Activa Bioactive Restorative całkowicie wyczerpuje definicję szeroko rozumianych kompozytów, z drugiej jednak strony takie zaszufladkowanie tak odmiennego tworzywa można uznać za krzywdzące.
Nowatorski na każdym etapie materiał oprócz tego, że zawiera bioaktywny napełniacz, podczas polimeryzacji tworzy hydrofilową matrycę, a dodatek elastycznych monomerów kauczukowych czyni zeń w pełni odmienne tworzywo odtwórcze. Przyjazna estetyka oraz podwójny sposób aktywacji polimeryzacji stanowią dodatkowe zalety, co pozwala bezsprzecznie dopisać również klasyfikację Bulk Fill.
Zespół Martínez-Sabio i wsp., porównując dwa nowoczesne kompozyty i dwa materiały Bulk Fill, potwierdził wyższą od materiałów kompozytowych typu Bulk Fill szczelność brzeżną i zbliżone wartości siły łączenia do uzyskiwanych przez kompozyty nanohybrydowe.
Opracowanie Sajini, Alshawi i Alharbi wskazało na wyższe uwalnianie jonów Ca i P przez Activę w porównaniu z Beautifil II i Fuji IX, przy zachowaniu większej twardości powierzchni.
Activa do wykonywania wypełnień stałych występuje obecnie w dwóch odmiennych wersjach: jako opisana już Activa Bioactive Restorative oraz nowsza, wyłącznie światłoutwardzalna Activa Pronto. Oba tworzywa podczas aplikacji charakteryzuje niska lepkość, co pozwala na aplikację metodą tradycyjną, jak również „flow iniection”. Dopełnieniem tej linii produktów jest Activa Kids (do wypełnień w zębach mlecznych) oraz Activa cement i podkładowa Activa Base/Liner. W opinii autora dwa pierwsze materiały wypełnieniowe nie mają obecnie zamienników w ofercie innych producentów. Liczne opracowania oceniają efektywność materiału w leczeniu ubytków zębów stałych, a badanie kliniczne Lardani i wsp. potwierdziło skuteczność materiału Activa Bioactive w leczeniu ubytków na powierzchniach żujących i stycznych zębów mlecznych.
Uszczelniacze kanałowe, uszczelniacze bruzd i materiały podkładowe
Dopełnieniem grupy materiałów bioaktywnych stosowanych w stomatologii zachowawczej będą uszczelniacze kanałowe, uszczelniacze bruzd i materiały podkładowe. W grupie tych ostatnich jako tworzywo do pokrycia bezpośredniego i pośredniego w opracowaniach prym wiedzie MTA, co jest skutkiem najdłuższego okresu obserwacji i liczby dostępnych opracowań. Kolejno wspomnieć należy o Biodentine i rozwijającej się grupie materiałów światło- i światło-chemoutwardzalnych, które możemy zakwalifikować jako kompozyty, acz ze względu na skład i właściwości będą one stanowić całkowicie odrębną grupę.
W praktyce autora stosowane są m.in. trzy materiały z rodziny Thera®: TheraCal LC, TheraBase Ca oraz TheraCal PT. Wszystkie mają w składzie fotoinicjator, a dwa ostatnie – również aktywator chemiczny, co zapewnia pełną polimeryzację w miejscach o utrudnionym dostępie światła. Jedynie TheraBase Ca nie może być wykorzystywany do pokrycia bezpośredniego, natomiast doskonale sprawdza się jako podkład pośredni. Materiał TheraCal LC może sprawiać pewne trudności podczas stosowania z powodu słabego przylegania do podłoża. Podwójnie korzystnym rozwiązaniem jest pokrycie TheraCal LC materiałem TheraBase Ca. Ten drugi dzięki zawartości monomerów MDP uzyskuje znacznie większą siłę łączenia, ponadto w świetle analiz producenta taka „kanapka” dzięki kumulacji znacznie zwiększa uwalnianie jonów wapniowych – wartość jest blisko dwukrotnie wyższa po pokryciu TheraBase w porównaniu z nanokompozytem Filtek w okresie siedmiu dni od aplikacji. Ze względu na właściwości TheraCal PT jest przeznaczony do zabiegu pulpotomii, acz w praktyce znajduje znacznie szersze zastosowanie, także w pokryciu bezpośrednim i pośrednim miazgi w zębach stałych. Zabieg pulpotomii i wypełnienia ubytku w zębie mlecznym u malucha można z powodzeniem wykonać podczas jednej wizyty, jak również dwuetapowo. Zawsze jednak należy pamiętać o pokryciu powierzchni żujących wypełnieniowym materiałem kompozytowym.
Odnosząc się do biozgodności, to opracowanie Kunert i wsp. wskazuje na porównywalne wartości w ocenie toksyczności preparatów MTA oraz Activa Bioactive i Predicta Bioactive.
Zalety stosowania materiałów bioaktywnych
Kończąc tę ograniczoną rozmiarami publikacji prezentację materiałów bioaktywnych, przejdźmy do zalet wynikających z praktycznego ich stosowania.
Zasada uwalniania jonów z materiałów bioaktywnych, tworzenie roztworu przesyconego i możliwość dyfuzji do zdemineralizowanych tkanek stanowią mechanizm bioaktywności. Indukowanie wytwarzania kryształów hydroksyapatytu jest możliwe po spełnieniu podstawowych warunków. Utrudnienie migracji jonów poprzez zamknięcie bioaktywnych szkieł w szczelnej, hydrofobowej matrycy eliminuje praktycznie możliwość dyfuzji z masy materiału. Z drugiej strony brak szczelności ubytku może doprowadzić do ucieczki jonów ze środowiska reakcji, a niskie stężenie nie będzie powodowało remineralizacji. Uzyskanie szczelności brzeżnej zapewni system łączący przeciwdziałający naprężeniom skurczowym. Elastyczna matryca zawierająca monomery kauczukowe będzie sprzyjać relaksacji naprężeń, a dowiedziony półprzepuszczalny charakter bariery tworzonej przez bond nie przeciwdziała dyfuzji jonów. Odmienność składu systemów łączących, stopień nasycenia napełniaczem oraz wytwarzana grubość warstwy będą modyfikować ten istotny parametr.
Nie bez znaczenia pozostaje tu również skrupulatność stosowania zaleceń producenta w zakresie postępowania klinicznego. Optymalne warunki do wykorzystania potencjału bioaktywnego będą stwarzać rekonstrukcje wykonane z wykorzystaniem podkładów/ pokrycia z materiałów bioaktywnych przy nieco mniej istotnym znaczeniu zewnętrznej warstwy rekonstrukcji/ wypełnienia. Ta zewnętrzna warstwa ma za zadanie zapewnienie szczelności. Badania wskazują jednoznacznie, że nawet Activa Bioactive dla spełnienia tego warunku musi być stosowana wraz z systemem łączącym. Benetti i wsp. wykazali brak samoistnej adhezji tego materiału do twardych tkanek zębów.
Właściwości dostępnych materiałów pozwalają już na wykonywanie zarówno pełnych jednolitych bioaktywnych odbudów, właściwym więc będzie również wykonywanie wypełnień typu „kanapka”, i to zarówno zamknięta, jak i otwarta, przy zachowaniu troski o właściwy dobór stosowanych komponentów.
Opracowanie Sahoo i wsp. porównujące zmiany właściwości nanokompozytu ormoceru, kompomeru i Activa Bioactive Restorative po ekspozycji na działanie roztworów wykazały, że jedynie nanokompozyt (Z350 3M ESPE) przewyższał Activę wytrzymałością podczas oceny odporności na ścinanie. Jest to powiązane z zastosowaniem wysokiej zawartości nanonapełniacza oraz monomeru Bis-EMA w matrycy. Jest to okupione jednak jej właściwościami hydrofobowymi w odróżnieniu od hydrofilowej matrycy Activy.
Porównanie wrażliwości na pH ekspozycji wskazuje na celowość zastosowania zewnętrznego okrycia Activy uretanowym materiałem nanokompozytowym przy stwierdzonym ryzyku narażenia na zwiększoną ekspozycję na działanie środowiska kwaśnego (refluks, zespół bulimia–anoreksja). Wszystkie oceniane parametry szeregowały Activę powyżej parametrów testowanego kompomeru (F2000 3M ESPE).
Wybór materiałów
W praktyce klinicznej uzyskanie optymalnego efektu terapeutycznego wymaga zarówno sprawności operatora, jak i biegłości w pracy stosowanymi materiałami, których dobór musi poprzedzać dokładne zaznajomienie się z zaleceniami, zakresem wskazań i przeciwwskazań. Wybór optymalnego preparatu jest łatwy, ale zmienność napotykanych klinicznie wyzwań wymaga posiadania kilku materiałów o odmiennych właściwościach.
I tak w przypadku pokrycia pośredniego autor preferuje preparat LimeLite, który oprócz przyjaznej w porównaniu z TheraCal LC estetyki jest również znacznie łatwiejszy w zastosowaniu. Tu jednak wspomnieć należy – co może dla wielu będzie truizmem – że nie jest łatwym określenie grubości warstwy zębiny oddzielającej nas od miazgi, ale cienka czerwona linia niechaj pozostanie na półce z książkami, a nie wkracza do praktyki.
Decyzja o stosowaniu Activy Bioactive Restorative czy Activy Pronto jest podyktowana zarówno rozległością ubytku, jak i szczególnymi warunkami estetycznymi. Nie ma też ograniczeń w łączeniu tych tworzyw. Szeroka gama kolorów Activy Pronto czyni zeń materiał uniwersalny, choć właśnie ciemne kolory, np. A4 i A6, doskonale zwiększają zakres zastosować w gerostomatologii. Ciekawą i nieco onieśmielającą na początku pracy tym materiałem cechą jest istotna zmiana zabarwienia materiału podczas polimeryzacji. Kolor ostateczny osiąga on dopiero po pełnej polimeryzacji światłem. Doskonała adaptacja brzeżna sprawia, że nawet nieprecyzyjnie dobrane zabarwienie zostanie praktycznie zamaskowane.
Opisywane w jednej z publikacji nieco gorsze parametry zużycia trybologicznego dla materiału Activa Bioactive Restorative w porównaniu z analizowanymi nanohybrydami należy rozpatrywać w kategoriach oceny laboratoryjnej. Z definicji odporności trybologicznej wynika, że zużycie ścierne nie jest cechą materiału, tylko charakteryzuje warunki prowadzenia eksperymentu.
Dotychczasowa subiektywna ocena kliniczna potwierdza wysoką skuteczność zarówno klasycznej Activy Restorative, jak i młodszej wersji Pronto, a ze względu na właściwości bioaktywne niezmiennie pozostają one materiami kompozytowymi o szczególnych właściwościach – materiami do zadań specjalnych.
Podsumowanie
Do niedawna uznawano, że stosowanie wypełnień kompozytowych powinno mieć miejsce dopiero po utrwaleniu prawidłowych nawyków higieny jako gwarancja powodzenia terapii. Właściwości, jakie oferuje bioaktywny materiał odtwórczy, pozwalają na zabezpieczenie leczonego zęba materiałem bioaktywnym, a jednocześnie uzyskanie estetycznego i trwałego wypełnienia ostatecznego podczas jednego zabiegu. Postęp technologii materiałowej pozwala na usprawnienie i uproszczenie postępowania przy zapewnieniu maksymalnego bezpieczeństwa wdrażanej terapii.
To właśnie ten dynamiczny rozwój technologii i doskonalenie zawodowe stomatologów sprawiają, że nie jest planowane otwieranie kilkudziesięciu nowych uczelni, jak ma to miejsce w odniesieniu do lekarza medycyny.